Laënnec lui a donné son nom en 1819 (en grec Kiros = roux) car le foie cirrhosé prend une couleur rousse pathologique. Les français l’ont adopté, car que la cause soit l’alcool ou les hépatites virales, 15000 personnes par an décèdent des suites d’une cirrhose. La cirrhose est l’aboutissement d’une lente transformation du foie par la fibrose. L’architecture du foie est désorganisée, il devient dur avec des nodules qui gênent puis empêchent sa circulation sanguine et il n’est plus apte à remplir ses multiples fonctions (stockage, tri, transformation, épuration, redistribution)
Les principales causes de cirrhose de l’adulte
Ce sont l’alcool pour plus de 75% (associé dans au moins 10% des cas à une hépatite C), les hépatites chroniques C (20 à 25%) et B (5%), et les autres causes (l’hémochromatose génétique (surcharge de fer dans le foie), les cirrhoses biliaires, les hépatites auto-immunes, la maladie de Wilson) représentent 5% des cas. L’hépatite chronique C est aussi la 2° cause de cancer du foie, juste derrière l’alcool.
Les cirrhoses dues aux hépatites chroniques sont la 2ème cause de transplantation hépatique en France, elles jouent au coude à coude avec la cirrhose alcoolique qu’elles tendent à rattraper, surtout lorsqu’un cancer se greffe sur la cirrhose virale.
Fréquence de la cirrhose dans les hépatites chroniques
Tous les porteurs d’hépatites devenues chroniques ne développent pas de fibrose et / ou de cirrhose. La proportion de porteurs d’hépatite chronique C qui vont atteindre le stade de cirrhose est estimée à 20-25%. Pour les hépatites actives B, la fréquence de la cirrhose serait d’environ 5% (elle varie selon le type du virus, mutant ou non).
La fibrose du foie dans les hépatites chroniques C
Le foie est le principal site de production de virus (environ mille milliards de virus par jour) mais également leur principale victime. Les hépatocytes infectés présentent à leur surface des protéines virales qui vont être détectées par le système immunitaire. Ces hépatocytes sont identifiés comme des ‘’étrangers’’ et donc détruits impitoyablement. Cette réaction entraîne des lésions inflammatoires et une surproduction de fibres de collagène qui s’accumulent entre les hépatocytes et les étouffent. Les cellules ‘’travailleuses’’du foie meurent et sont remplacées par du tissu cicatriciel fibreux qui lui ne fait rien d’utile.
Il s’agit donc au début d’un mécanisme physiologique de cicatrisation. La fibrose est une cicatrisation pathologique lié à la persistance du virus dans le foie et à l’entêtement du foie et du système immunitaire à vouloir l’éliminer.
Dans l’hépatite B, la cirrhose finale est sensiblement la même, les complications aussi, mais l’hépatite B évolue souvent par poussées successives.
Evolution de la fibrose
L’évolution de la fibrose et sa vitesse de progression vers la cirrhose sont très variables selon les individus : les ‘’fibroseurs rapides’’ peuvent avoir une cirrhose en moins de 20 ans, voire moins de 10 ans, les ‘’fibroseurs lents’’ mettront 40 ans ou plus pour y arriver et pour les ‘’fibroseurs intermédiaires’’, le délai est d’environ 30 ans.
- La progression plus ou moins rapide de la fibrose est liée à plusieurs facteurs dont certains sont corrigibles (l’alcool surtout):
- L âge : s’il est supérieur à 40-50 ans à la contamination, la fibrose évolue plus vite
- La consommation d’alcool : l’alcool est un facteur multipliant par 7 le risque de fibrose au cours de l’hépatite virale. Lorsque la fibrose est initiée, l’alcool double ou triple la vitesse d’installation de la cirrhose (même en quantité modérée). Logique car on cumule alors les 2 grandes causes de cirrhose.
- Le sexe masculin : les hommes ont une évolution vers la cirrhose plus rapide. Les femmes bénéficieraient du pouvoir anti-fibrosant des hormones féminines.
- La co-infection avec le VIH : elle accélère beaucoup (de 2 à 3 fois selon les études) la vitesse de la fibrose, surtout si les CD4 sont bas. Le taux de virus C dans le sang est plus élevé. La réponse au traitement du VHC est moins bonne. Certains anti-rétro-viraux utilisés pour le VIH peuvent augmenter’’ la souffrance’’ des hépatocytes.
- La stéatose (graisse envahissant le foie), la stéatose semble plus fréquente en cas de génotype 3 du VHC, par un effet direct du virus, mais elle ne semble pas jouer sur la fibrose. Pour les autres génotypes du virus (1a, 1b, 2, 4, 5, 6) la stéatose serait la conséquence indirecte des perturbations lipidido-glucidiques observées en cas de surpoids et/ou de diabète, ainsi que lors de la co-infection avec le VIH (par les complications métaboliques dues aux traitements) et elle contribue à la cirrhose.
- Le fer : La surcharge du foie en fer est fréquente (surtout chez les hommes) mais modérée et elle aggrave les lésions histologiques.
- Les facteurs viraux, charge virale et les différents génotypes ne semblent pas intervenir directement sur l’évolution de la fibrose.
Pour les hépatites chroniques B, les facteurs de progression sont les mêmes qu’avec le C, avec en plus la co-infection par le virus Delta, délétère et les réactivations.
Évaluation de la fibrose
Elle est nécessaire pour connaître le stade de la fibrose et son évolution. Mesurer la fibrose revient à mesurer les conséquences de l’hépatite sur le foie, car la prise en charge et les traitements varient. Il existe plusieurs scores d’évaluation et plusieurs méthodes pour arriver à ces scores
La Ponction Biopsie Hépatique (PBH) : une petite ‘’carotte’’ de foie est ponctionnée à travers deux côtes, de 10 à 20 mm, et examinée au microscope par des histologistes. La PBH reste la méthode de référence pour évaluer les stades d’inflammation et de fibrose, mais c’est un geste invasif qui comporte des risques rares mais réels (hémorragie, plaies des voies biliaires, du rein…). Ce risque diminue lorsque la PBH est écho-guidée (avec une échographie qui visualise les organes)
En cas de troubles de la coagulation, la PBH se fait par voie trans-jugulaire.
Le score METAVIR est le plus utilisé. Il classe l’activité (c’est-à-dire l’ensemble des lésions de nécrose et d’inflammation) en 4 stades et la fibrose en 5 stades (de Fo à F4)
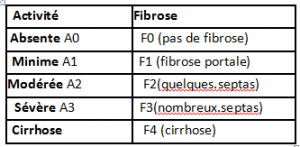
La fibrose portale : elle se trouve autour des espaces portes (1), sans déborder
Les septas sont des ‘’ponts’’ de fibrose entre les espaces portes
La cirrhose est le stade le plus avancé, soit A3F4, la fibrose a tout envahi.
Le score de KNODELL est plus ancien, plus général car il ne dissocie pas vraiment l’activité et la fibrose et donne un résultat ‘’en bloc’’, de 0 à 22 points.
Le score d’ISHAK, plus précis, comporte 6 stades pour la fibrose. Il est moins utilisé car beaucoup plus long et plus compliqué à lire pour les anatomopathologistes. Il est considéré comme le meilleur et les hépatologues pensent qu’il y aurait moins d’erreurs sur le rendu des résultats avec ISHAK.
Les marqueurs sériques de fibrose
Il en existe plusieurs, français et européens, et ils ont longtemps été attendus impatiemment par les patients lassés de la répétition des biopsies, qui paraissent bien lourdes à coté d’une simple prise de sang.
Le test le plus connu et le plus utilisé en France est le Fibrotest-Actitest® : mis au point en 2001 par l’équipe du Pr Thierry Poynard (Pitié-Salpêtrière, Paris), cet index de fibrose combine le dosage dans le sang de cinq marqueurs indirects de fibrose hépatique (alpha-2 macroglobuline, haptoglobine, apolipoprotéine A1, bilirubine totale, gamma-GT)) ajustés à l’âge et au sexe. On obtient des chiffres ‘’traduits’’ en METAVIR : ex : un score d’activité de 0,20 = A0-A1 et un score de 0,35 = F1-F2.
Ce test est maintenant remboursé en grande partie (en ville, reste a charge de 20 Euros) et gratuit lorsqu’il est fait à l’hôpital.
Ce test est très apprécié des patients mais il leur rend parfois un résultat catastrophique
(A3-F4), inexact, brouillé par une élévation d’un ou plusieurs marqueurs pour une autre cause. Ceci est surtout vrai dans la co-infection, car certains anti-rétroviraux peuvent élever la bilirubine (Reyataz®, Crixivan®), d’autres font monter les transaminases (les antiprotéases, Viramune®, Videx®, Zérit®) et la biopsie doit être faite pour trancher.
Le Fibrotest® peut aussi rendre des résultats ’’trop bons’’ dans 20% des cas.
Pas de jaloux, la biopsie aussi peut donner des résultats sous ou sur-estimés.
La ponction peut être faite dans un des seuls endroits encore sains d’un foie bien décrépit ou le contraire, mais c’est surtout sur la taille de la ‘’carotte’’ et sur la lecture de la lame que les avis divergent. Certains hépatologues crient haut et fort qu’il faut des prélèvements plus grands, de 25 mm, comprenant plus d’espaces portes pour être sûr de ne pas passer à côté de la vérité. Les anatomopathologistes ‘’experts du foie’’ disent qu’ils trouvent beaucoup d’erreurs (de 1 à 2 grades du A et du F !) quand ils ‘’relisent’’ des lames de biopsies lues dans des centres non-experts…L’idéal pour éviter les PBH répétées et pouvoir croire au résultat serait de faire au moins une biopsie hépatique et un Fibrotest® en même temps et si les résultats sont concordants, le suivi de l’évolution peut alors se faire par des Fibrotests®
La méthode la moins invasive : le Fibroscan
Le Fibroscan utilise une technologie brevetée, l’élastométrie impulsionnelle. Celle-ci consiste à engendrer une petite vibration à la surface de la peau qui va se propager jusque dans le foie. Avec des ultrasons, on en mesure la vitesse. Plus cette vibration se déplace rapidement, plus le foie est dur. Le Fibroscan mesure donc la dureté du foie. Plus le foie est dur, plus il est fibrosé. Actuellement, tous les centres hospitaliers français avec un service d’hépatologie disposent de l’appareil et effectuent ces mesures. Son défaut :il voit bien les foies ‘’mous’’(pas de fibrose), les foies ‘’durs’’(très fibrosés) mais les stades intermédiaires ne sont pas son fort.
Classification de la cirrhose
Une cirrhose annoncée, A3-F4 par METAVIR doit être confirmée et évaluée par des examens complémentaires car la cirrhose aussi doit être classifiée pour suivre son évolution (recherches de signes cliniques et biologiques et examens exploratoires).
L’examen clinique peut trouver à la palpation une hépatomégalie (gros foie) dure à bord inférieur tranchant, lisse ou granuleuse ou un foie de taille normale ou atrophique.
Les signes cliniques d’insuffisance hépatique (si plus de 75% du foie est fibrosé) :
– les angiomes stellaires ou taches colorées en forme d’étoiles sur le visage, le thorax et les bras, l’érythrose palmaire (teinte rosée de la paume des mains), les ongles blancs et striés, l’asthénie, l’ictère (teinte jaune de la peau et du blanc des yeux), une grosse rate, l’encéphalopathie hépatique (confusion mentale transitoire due à l’accumulation de toxines que le foie n’arrive plus à éliminer) ;
– les examens biologiques montrent souvent une neutropénie, une thrombopénie (baisse des globules blancs et des plaquettes), parfois une anémie, la bilirubine est normale ou augmentée, les transaminases (ASAT et ALAT) et les gamma-GT sont augmentées, l’albuminémie et le taux de prothrombine (TP) sont diminués.
– L’alfa-foetoprotéine, le marqueur du cancer du foie fait partie du bilan. Il est fiable à 75% pour les grosses tumeurs, mais seulement à 25% pour les petites tumeurs.
– L’échographie abdominale sert à apprécier le volume du foie, les modifications de sa forme et de sa structure. Elle montre aussi les signes d’hypertension portale (HTP) (dilatation des veines hépatiques et présence de voies de dérivations veineuses, ascite) et recherche une tumeur. Selon les résultats, il peut être nécessaire d’explorer une lésion par un scanner, pour mieux voir les vaisseaux du foie ou par une IRM, encore plus précis pour les tumeurs.
– La fibroscopie gastrique recherche les signes d’HTP, les varices oesophagiennes ou gastriques.
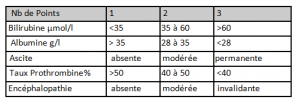
La classification de Child-Pugh note la gravité de la cirrhose.
C’est un score clinico-biologique, qui définit 3 stades de gravité croissante, en totalisant des points sur le tableau : stade A : 5 à 6 points, B : 7 à 9, C : 10 à 15 points
Le stade A de Child-Pugh correspond à la cirrhose “compensée”, état où la cirrhose n’a pas de manifestations cliniques, ni de complications, ce stade pouvant durer des années, surtout avec une bonne hygiène de vie (sans alcool+++) et avec un bon suivi.
Le stade A correspond à une insuffisance hépatique légère, le B à une insuffisance modérée et le C à une insuffisance sévère avec décompensation.
Le suivi de la cirrhose : du sur-mesure :
La fréquence des examens, la décision de commencer un traitement ou de le retenter après un échec, la mise en route d’un traitement d’entretien (petites doses d’interféron) dépendent des résultats, de l’évolution ou de la stabilisation de la cirrhose, du moral du patient et du punch de son médecin qui doit lui même y croire pour convaincre.
La fibrose est réversible, une ‘’jeune’’ cirrhose peut régresser si le virus est éradiqué par le traitement Peg-interféron+ribavirine. Même en cas d’échec sur le virus, le traitement a un effet sur la fibrose.
Les médicaments anti-VIH doivent être dosés dans le sang car une dose plus faible suffit souvent à contenir le virus et limite les effets indésirables.
Système D : Les médecins sont obligés de faire preuve d’imagination et d’audace pour essayer de stabiliser la cirrhose. Braver l’AMM et les standards est l’exercice quotidien de certains. Par exemple, pour donner plus de chance au traitement de l’hépatite C dans le cas de patients qui n’arrivent pas à s’abstenir d’alcool, certains médecins essayent le Subutex®, qui permet souvent un arrêt de l’alcool (surtout chez les ex-toxicomanes qui se sont substitués eux-mêmes par l’alcool). Le Zyban® a été essayé et maintenant le baclofène et le nalméfène qui chez certains permet un arrêt ou du moins une diminution de la consommation d’alcool.
Le Peg-interféron a été utilisé dans l’hépatite B active ou en cirrhose alors qu’il n’avait pas encore l’AMM pour cette indication.
Les médicaments à effet anti-fibrosant, anti-stéatose sont évalués par des essais cliniques, mais aussi en ‘’sauvage’’, en anticipant les résultats. C’est le cas de la pentoxifylline (vasodilatateur ayant un effet anti-TNFα), de la colchicine (anti-goutteux), de l’acide ursodésoxycholique (traitant les lithiases biliaires), le pirfenidone (anti-fibrose), de la vitamine E (anti-oxydant limitant la stéatose)
Les patients aussi appliquent le système D, en cherchant l’information (associations de patients, internet), en échangeant des tuyaux, des expériences, des adresses. Ils trouvent eux-mêmes des produits anti-fibrosants, hépatoprotecteurs, produits que l’on retrouve dans un sérieux livre de l’Inserm (2) sur les dégâts de l’alcool, apparemment non dangereux et pouvant être bénéfiques. Il s’agit de la méthionine, un acide aminé qui se transforme en S-adénosylméthionine (SAM) et de la phosphatidylcholine (la lécithine de soja). Leur rôle hépatoprotecteur viendrait du fait qu’ils augmentent la production de glutathion, puissant anti-oxydant qui combat le stress oxydatif et protège les mitochondries (les fabriques d’énergie des cellules), et diminuent la stéatose.
La N-acétyl-cysteïne augmente aussi le glutathion et se trouve en pharmacie car c’est aussi un fluidifiant bronchique.
La silymarine (extrait du chardon-marie) est également utilisée pour son action anti-fibrosante (diminue la synthèse du collagène). Les vitamines C et B sont utiles.
La cirrhose, à désamorcer aussi dans la tête
Lorsque le patient apprend qu’il a une cirrhose, il est primordial de lui proposer un soutien psychologique et/ou un partage avec d’autres patients (groupes de parole)
Avec le temps et un pouvoir d’adaptation élastique, l’hépatite C ou B, la co-infection peuvent être acceptées et intégrées dans une vie et un esprit remodelés.
Mais la cirrhose est vécue souvent comme une énorme injustice (mais je ne bois pas !),le patient peut alors baisser les bras en pensant que c’est la fin du voyage.
Les hépatites, leurs traitements, la rechute, la cirrhose nécessitent de l’information, des conseils, un partage pour être acceptés et pris en charge aussi par le patient qui ne doit pas rester spectateur de sa maladie mais bel et bien le principal acteur. Certains actes, décisions ne peuvent être prises que par lui (arrêt de l’alcool, commencer le traitement)
La cirrhose peut devenir une leçon de vie, un espace-temps pour réfléchir, s’informer, réagir. Pour pouvoir de nouveau anticiper son avenir, la traversée de ce pont suspendu entre deux vies est nécessaire et une fois arrivé, l’espoir doit se cultiver tous les jours.
Pour la cirrhose due au VHC, de nouvelles molécules antivirales directes sont maintenant à disposition pour les cirrhotiques et certaines sont en AMM et elles tiennent leurs promesses face à des virus qui ont résisté aux traitements antérieurs (interféron, bithérapie, trithérapie avec les IP de 1ère génération).
Marianne. L’HENAFF
(1) Espaces portes : espaces situés aux angles de chaque lobule du foie, à travers lequel passent une veinule issue de la veine porte, une artériole de l’artère hépatique et un (ou deux) canal biliaire.
(2) Expérience collective, Alcool – Effets sur la santé, Inserm 2001