Les virus des hépatites B et D (Delta) sont responsables au niveau mondial de deux millions de décès chaque année. Si la population générale a déjà entendu parler des hépatites B et C, l’hépatite delta est quasi inconnue.
Les médecins et les firmes pharmaceutiques considèrent l’hépatite Delta comme un appendice de l’hépatite B (le virus D n’infecte que des personnes porteuses du virus de l’hépatite B), laissée de côté car elle touche relativement peu de personnes dans les pays nantis (essentiellement des toxicomanes et des homosexuels), en comparaison avec les hépatites B seule ou C. Il n’y a donc pas ou peu de recherches, de protocoles ni de réponse thérapeutique satisfaisante pour la D. L’hépatite D, comme délaissée ? C’est une aberration, vu la gravité de l’atteinte hépatique qu’elle peut causer, et le CHV (1) souhaite qu’elle soit reconnue comme une maladie orpheline, pour que des centres de références existent pour cette hépatite mal connue, mal soignée le plus souvent.
Il n’y a pas de vaccin spécifique anti delta, mais comme le virus D ne se développe que chez des sujets porteurs du virus B, la vaccination contre le virus de l’hépatite B protège donc aussi du virus de l’hépatite D.
A, B, C, D…
Il est probable que les hépatites virales existent depuis la Haute Antiquité. Le premier traité de médecine, écrit en 3 000 avant J-C, faisait déjà état de la jaunisse, symptôme principal de l’hépatite aiguë. À ce jour, plusieurs virus infectieux pour le foie et pouvant donner une hépatite ont été identifiés : A, B, C, D, E, G sont les principaux.
Le virus de l’hépatite D (VHD) a été découvert en 1977 par Mario Rizzetto, jeune gastro-entérologue de l’hôpital Molinette de Turin (Italie). Travaillant sur des biopsies hépatiques de patients souffrant d’hépatites virales chroniques B particulièrement sévères, il a mis en évidence dans le noyau des hépatocytes un nouvel antigène, qu’il a nommé antigène delta.
Le virus Delta, un virus ‘’naturiste’’
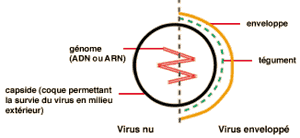
Le virus de l’hépatite delta ou D (VHD) est un agent infectieux très spécial car il est « nu », sans enveloppe. Le VHD est composé d’un ARN circulaire en simple brin et d’un antigène delta, fixé au génome du virus. Il a le plus petit génome de virus connu.
Le VHD est un virus « défectif » car il a absolument besoin de la présence du virus de l’hépatite B (VHB) pour fonctionner. Le virus D est «tout nu» et il se sert de l’enveloppe du VHB pour devenir un « vrai virus » bien méchant. Le VHD a une réplication autonome, mais en l’absence d’infection par le VHB qui lui fournit une enveloppe décente, les particules virales du VHD ne peuvent pas « sortir » de la cellule hépatique et le VHD est alors très peu pathogène. Le virus Delta est un virus satellite du VHB, ‘’un chiffonnier’’ récupérant les vieilles enveloppes vides de la B pour l’assemblage final de ses particules infectieuses, enveloppes produites en grande quantité chez les porteurs chroniques de l’antigène HBs (hépatite B chronique active). Le virus D a une double enveloppe à sa sortie de la cellule hépatique, l’enveloppe externe est constituée d’antigène HBs du VHB. La synthèse de l’enveloppe interne, formée par l’antigène delta dépend du génome du virus delta.
Structure du virus D, nu et avec enveloppe…
Prévalence et épidémiologie du VHD (ou combien, chez qui et où…)
À l’échelle mondiale, plus de 5 % des personnes infectées par le virus de l’hépatite B le sont aussi par celui de l’hépatite D. Dans certains pays, ce pourcentage va jusqu’à 20%. Les chiffres donnés lors de la conférence de consensus sur la co-infection en 2005 (2) étaient de 400 millions de porteurs chroniques du VHB dans le monde, soit donc plus de 20 millions de personnes infectées par le VHD également. En 2013, l’OMS avançait plutôt 250 millions de porteurs de VHB (niveau mondial) et donc de 10 à 15 millions de porteurs « doubles » de VHD et VHB. L’épidémiologie du VHD montre des zones d’endémie dans le bassin méditerranéen (sud de la France, Italie, Grèce), dans certaines régions d’Europe de l’Est (Roumanie, ex-Yougoslavie, Albanie), du Proche-Orient, de l’Inde, dans certains pays d’Afrique (Afrique du Nord) et d’Amérique latine (Venezuela, Colombie, Pérou). De graves épidémies d’hépatite delta ont été observées à Naples en 1977, chez les Indiens Yupca du Venezuela en 1981, en Colombie, au Brésil et enfin en République Centre africaine. Le VHD se décline en trois principaux génotypes. Le génotype I est le plus courant dans le monde, mais le génotype II prédomine à Taiwan. (La maladie associée au génotype II serait moins sévère que le génotype I) et le génotype III est associé à des éruptions d’hépatites ‘’sévères’’ au Venezuela et au Pérou.
Modes de transmission du VHD
Dans les régions de faible endémie, la transmission parentérale (par le sang) du VHD est la plus fréquente et concerne les groupes à risque d’infection pour le VHB. Elle s’effectue par les produits sanguins (hémophiles, hémodialysés et transfusés) et les partages de seringues chez les toxicomanes (risque élevé chez les toxicomanes). Des épidémies d’hépatites D fulminantes ont été décrites chez les toxicomanes des États-Unis et d’Europe de l’Ouest. La transmission s’effectue aussi par voie sexuelle (comme et souvent avec le VHB, homosexuelle surtout) et de la mère à l’enfant. La transmission par la salive reste controversée. Les lésions cutanées des enfants (impétigo, gale, maladies de peau) peuvent favoriser la transmission du VHD. Des cas de contaminations intrafamiliales ont été décrits en Italie.
Gravité
Lors des doubles infections VHB-VHD, le pronostic d’une hépatite B est aggravé par le VHD, avec davantage de complications et une évolution plus rapide de la maladie. Les hépatites chroniques D évoluent vers la cirrhose dans 60 à 70% des cas, et plus rapidement.
La contamination par le virus D
Les personnes infectées par le virus de l’hépatite D peuvent être co-infectées (infectées par le virus de l’hépatite B et celui de l’hépatite D en même temps) ou surinfectées (personne déjà infectée par le virus B puis contaminée par le virus D ensuite, lors d’une nouvelle prise de risque (sexuelle ou sanguine)).
Les symptômes cliniques et biologiques, le passage à la chronicité sont différents selon le mode de contamination du VHD, immédiat ou différé de l’hépatite B. La période d’incubation du VHD est plus longue dans les cas de co-infection que de surinfection.
> La contamination simultanée VHB/VHD
- Son incubation est de 5 à 12 semaines. Lors de cette co-infection, les signes cliniques sont souvent absents, comme pour la plupart des hépatites aiguës B (c’est-à-dire le plus souvent sans manifestations cliniques). Seuls les signes biologiques (élévation transitoire des transaminases hépatiques (ASAT, ALAT) et sérologiques témoignent de l’infection. Puis cette infection guérit spontanément dans 95% des cas. Le VHD n’augmente pas ou peu le risque d’évolution vers le stade chronique du VHB. Il reste de 5%. Ces 5% restants deviennent des porteurs chroniques du VHB et du VHD, avec un risque plus élevé de cirrhose et de cancer du foie.
- Cette hépatite aigue peut être symptomatique dans 10% à 20% des cas. Le diagnostic est facile en cas d’ictère (jaunisse), précédé souvent d’une forte fièvre. A la phase ictérique, les urines sont foncées (‘’bière brune’’), les selles décolorées (couleur mastic) et la fatigue intense. Le prurit (démangeaisons) est inconstant. Au cours d’une hépatite aiguë bénigne, l’ictère disparaît après 2 à 6 semaines. La fatigue peut durer jusqu’à trois à quatre mois. Les formes asymptomatiques (non ictériques) sont les plus fréquentes (80 à 90%), avec des signes non spécifiques, mais prolongés (plus de 3 à 7 jours). Ce sont des signes d’allure grippaux, de l’asthénie, des douleurs abdominales, des maux de tête, des nausées, de l’anorexie, de l’urticaire et des douleurs articulaires. -Le diagnostic repose sur la notion de contage (possibilité de transmission, de qui, quand, comment…), l’élévation des transaminases (à plus de 10 à 100 fois la limite de la normale) et les examens sérologiques. Deux pics distincts d’élévation du taux des transaminases, séparés de deux à cinq semaines peuvent être observés dans 10 à 20% des co-infections. La proportion de ‘’guérisons’’ est la même (95%) que les infections aigues sans symptômes.
- Mais la double infection VHB/VHD génère par contre une proportion importante d’hépatites fulminantes (17%), très graves, caractérisées par la survenue d’une encéphalopathie (troubles de la conscience allant jusqu’au coma) et responsables de la destruction de l’ensemble des cellules hépatiques en quelques jours. L’hépatite fulminante est fatale dans 80 à 90 % des cas. Seule une transplantation hépatique d’extrême ‘’super urgence’’ peut sauver le malade. Il existe une liste d’attente prioritaire pour ces cas d’hépatites fulminantes mais l’évolution fatale est souvent plus rapide que la liste et les transplanteurs.
> En cas de surinfection Delta
Au cours d’une surinfection (d’abord le VHB, devenu chronique, puis nouvelle prise de risque – sexuelle ou sanguine – et contamination par le VHD) la multiplication du VHD est massive et les lésions hépatiques sont sévères. L’hépatite aiguë est souvent symptomatique (ictère) chez 50 à 70% des patients. Une hépatite fulminante peut également se produire (en Italie, 42 % des hépatites fulminantes seraient liées à la surinfection par le virus D). Le gros problème de la surinfection delta est le développement dans 90% des cas d’une hépatite chronique delta qui vient compliquer le VHB chronique, avec une évolution beaucoup plus rapide vers la cirrhose dans 60 à 70% des cas (dont 15% en 1 à 2 ans).
Diagnostic sérologique de l’infection :
Le diagnostic d’hépatite aiguë D repose sur la présence de l’antigène delta (mais l’antigénémie est très fugace, de une à quatre semaines).et celle des anticorps anti-delta de type IgM dans le sérum, 2 à 4 semaines après le début des signes), suivis parfois des IgG. Ces anticorps (AC) ne persistent que si l’infection devient chronique.
- En cas de co-infection aigue, on trouve les marqueurs de l’infection aiguë par le VHB (AgHBs, et AC IgM anti-HBc) et de l’infection aiguë par le VHD (AC IgM anti-D et IgG).
- En cas de co-infection chronique, on trouve les AC IgM anti-HBc, les AC anti-HBe et les AC IgM anti D et on trouve moins l’Ag HBs.
- En cas de surinfection aiguë, on trouve l’AgHBs, les AC anti-HBe, les IgM anti-D. les AC IgM anti Hbc et l’Ag-e sont négatifs.
– L’antigène HBs est positif dans la co-infection et la surinfection puis généralement, il devient non détectable car la présence du VHD inhibe le plus souvent la réplication du VHB et l’Ag HBe n’est plus détectable.
La persistance des IgM anti-D est prédictive de la chronicité (bonne corrélation avec la réplication virale) et une charge virale VHD positive 6 mois après la contamination signe le passage à la chronicité.
L’hépatite D doit être recherchée dans le contexte d’un portage de l’antigène HBs et une hépatite sévère ou chronique sans signe de réplication du VHB (inhibition de la réplication du VHB car antigène HBe et ADN viral négatifs) et inversement, ces marqueurs peuvent persister et masquer l’hépatite D.
Chez les toxicomanes, l’infection par le VHD (et donc VHB) est souvent associée à une infection par le VHC et/ou par le VIH et il s’accompagne d’une diminution, voire d’un arrêt de la multiplication du VHC et du VHB.
Traitement
Actuellement il n’y a aucune thérapie antivirale spécifique efficace disponible pour le traitement de l’hépatite aigue ou chronique D. Les options thérapeutiques pour l’hépatite D chronique restent limitées, souvent à l’interféron…
Les analogues nucléosidiques et nucléotidiques contre le VHB ne sont pas actifs contre le VHD, mais la réponse du VHB aux traitements divers (Zeffix, Baraclude, Viréad, Hepsera…) joue un rôle dans son « avenir ».
Le taux d’ARN du VHD est désormais remboursé par les organismes de protection sociale. Ce test est essentiel pour évaluer la charge virale (CV) du VHD. Son taux et les autres marqueurs directs du VHD (Ag-HD) et indirects (anticorps de type IgG ou IgM anti-HD) permet de déterminer l’urgence ou non d’un traitement par interféron, sa réponse, sa durée…
L’interféron alpha standard a été utilisé avant le Peg dans l’infection chronique D et il devait être poursuivi longtemps (24 mois, voire plus), pour espérer un résultat favorable. Après 3 à 6 mois d’interféron, l’ARN du virus delta devient souvent indétectable, mais des rechutes sont souvent observées à la fin du traitement. Néanmoins, des rémissions à long terme ont été observées avec ce traitement, avec une régression de la fibrose hépatique vue à la biopsie (3).
Une réponse soutenue n’est possible que si l’AgHBs du VHB disparaît aussi. Le traitement doit être poursuivi si l’AgHbs persiste, même sans réplication détectable du virus delta. Environ 50% des porteurs chroniques répondaient à l’interféron 9 MU 3 fois par semaine (ou 5 MU quotidiennement) pendant 12 mois, mais le virus n’est pas éliminé par ce traitement. C’est au mieux une rémission. Le Peg-Interféron a été utilisé plus tard, à partir de l’année 2000. Dans une étude sur 14 patients, il a donné une réponse virologique prolongée chez 46% des patients (4), mais il y a eu des rechutes et au total, après retraitement par peg-INF, 5 patients sur 14 ont eu une réponse virologique soutenue (RVS).
D’autres études utilisant le Peg interféron α, aux posologies habituelles, ont montré des taux de réponse soutenue d’environ 20% après un traitement d’un an (5). Des études avec des traitements combinés d’IFN-α ou de PEG-IFN-α avec des analogues nucléosi/tidiques ou la ribavirine n’ont pas montré d’amélioration des taux de réponse par rapport à la monothérapie par IFN-α ou PEG-IFN-α seules (6) et (7). Des études sont en cours avec les récents analogues nucléosi/tidiques, plus puissants. Certains médecins se demandent si le vieil interféron (3 fois/semaine) ne donnerait pas de meilleurs résultats que le Peg-IFN, une revue de littérature des études (8) montrant que un traitement de 1 an à forte dose d’IFN-α en monothérapie semble être plus efficace que le PEG-IFN-α pour le traitement du VHD, avec des taux d’efficacité d’environ 30%.
Evaluation de la réponse au Traitement
Les critères d’évaluation du traitement sont encore mal définis. Les études avec le PEG-IFN-α ont défini une réponse à six mois après l’arrêt du traitement comme critère de réponse soutenue. Pour l’évolution à long terme, on ne dispose que de quelques données chez des patients traités par l’IFN-α.
Il est recommandé de déterminer l’ARN du VHD de manière quantitative tous les trois à six mois sous traitement. Il n’existe cependant pas de règles d’arrêt du traitement bien définies comme on les connaît pour le traitement de l’hépatite C. Une prolongation de la durée du traitement peut être décidée si l’on observe une réponse virologique tardive ou une reprise du traitement en cas de rechute.
Définitions de la réponse
- Réponse virologique précoce (RVP) = Diminution ≥ 2 log d’ARN VHD à la semaine 24 du traitement
- Réponse en fin de traitement = ARN VHD négatif en fin de traitement
- Non réponse (NR) = ARN VHD positif en fin de traitement
- Rechute = Réapparition d’ARN VHD après l’arrêt du traitement
- Réponse virologique soutenue (RVS) = ARN VHD négatif 24 semaines après la fin du traitement
Comme pour le VHC, la RVP à 24 semaines est prédictive de la réponse en fin de traitement et de la RVS (ARN VHD négatif 24 semaines après la fin du traitement).
Transplantation
La transplantation hépatique peut s’avérer nécessaire pour les patients VHD avec une cirrhose décompensée et/ou un CHC limité (un nodule de moins de 5 cm ou ≤ 3 nodules de moins de 3 cm, selon les critères de Milan). La récidive de l’infection par le VHB et, par conséquent, aussi par le VHD, peut être évitée de manière efficace grâce à une prophylaxie utilisant les immunoglobulines et les analogues nucléosi/tidiques.
Les patients avec cirrhose hépatique nécessitent une surveillance de dépistage de CHC, soit une échographie abdominale et une détermination de l’α-foetoprotéine tous les six mois.
Prévention
Il n’y a pas de vaccin spécifique contre le VHD. C’est la vaccination contre le VHB qui protège de l’infection à VHB et donc d’une infection VHD, de façon indirecte. Mais ni le vaccin anti-VHB ni les immunoglobulines anti-VHB ne permettent de prévenir l’infection à VHD chez les personnes atteintes d’une hépatite B chronique. Pour eux, préservatifs et seringues stériles sont la seule prévention.
Docteur, connaissez vous la Delta ?
L’hépatite D ne passionne ni les foules, ni les médecins, ni les laboratoires. Il n’y a pas de recherches, pas de traitements spécifiques, pas de conférences et même très peu d’articles sur cette mini-tueuse. Les porteurs de cette hépatite se sentent mis à part, au rencart total et éprouvent une légitime amertume de ce manque d’intérêt et de réponse des hépatologues qui se renvoient ces patients désemparés comme une patate chaude. Il n’existe même pas de cohortes des porteurs chroniques de la Delta, ce qui serait la moindre des choses. A une conférence sur les co-infections, pleine de centaines d’hépatologues, une question posée par un militant du CHV (1) sur la Delta a reçu la réponse ‘’il n’y a pas de spécialistes de la Delta dans cette salle !!’’
Les hépatologues sont ils devenus tellement spécialisés qu’ils ne traitent qu’une sorte d’hépatite ? Les malades ont besoin d’écoute, de soutien et surtout pas de dédain.
Marianne L’hénaff
Témoignage d’un Delta-Man, fait en 2005. Il est mort depuis de son hépatite delta, en 2010.
La Delta, ma pire ennemie
Mes trois virus (VIH, VHB, VHD) ont été dépistés en même temps, en 1991.
A l’époque, médecins et patients ne s’occupaient et ne flippaient que du VIH, le grand méchant terroriste. Pendant huit ans, j’ai pris les médicaments successifs pour le VIH (AZT, Videx, Zérit et Videx…) jusqu’à l’arrivée des anti-protéases en 96.
En 99, j’étais sous Epivir (entre autres) quand mes hépatites se réveillent hardiment. Ictère et transaminases élevées m’envoient chez l’hépatologue qui me propose un traitement par interféron après une biopsie indiquant une cirrhose (A3-F4). Il me dit que l’interféron est mieux supporté dans l’hépatite B que dans la C. Je fais ce traitement (interféron 3 fois par semaine) et me tape beaucoup d’effets indésirables (fatigue, anémie, dyspnée, maux de tête, sècheresse de la peau, irritabilité…). Les charges virales et les transaminases chutent, mais mon moral aussi. J’arrête de moi-même au bout de 9 mois, lessivé. Je reprends tant bien que mal ma vie. Deux ans plus tard, en 2002, elles sont remontées et l’hépato ‘’se débrouille’’ pour avoir de l’Adéfovir avant son agrément, qu’il me donne avec du Peg-interféron. Et rebelote, j’ai les mêmes effets indésirables qui me coupent du reste du monde, plus une décompensation de la cirrhose qui m’expédie à l’hôpital et de l’ascite qu’il faut ponctionner régulièrement. Une fois rétabli, j’obtiens un aménagement de mon poste, ce qui me permet de travailler surtout chez moi. En 2003, je fais une crise cardiaque et je bénéficie d’un triple pontage coronarien en urgence. J’avais du cholestérol et pourtant, je ne prends qu’une bithérapie de nucs (Viréad® + Epivir®), qui traite à la fois mon VIH et mon hépatite B et qui suffit à rendre le VIH indétectable. Comme quoi le méchant terroriste n’est pas celui qu’on croyait…
Pour vérifier que l’interféron agit sur la Delta, il faut faire des charges virales de la Delta avant, pendant et après le traitement. Jusqu’au début 2005 elle n’était pas remboursée par la sécurité sociale, l’hôpital se débrouillait avec ses budgets, ses enveloppes pour les faire. Un jour, trop crevé par l’interféron pour aller faire la prise de sang à l’hôpital à 7 h du matin, je l’ai fait dans le labo privé à côté de chez moi et là, j’ai payé cette charge virale 150 euros ! Maintenant, elle est remboursée (grâce à l’action insistante du CHV et du TRT-5) et c’est une libération pour moi de la faire à côté de chez moi.
Un Delta-Man qui garde l’espoir
Je viens de faire ma troisième cure d’interféron, avec des doses plus faibles (135 microgrammes). J’ai tenu un an. J’ai toujours de l’ascite, traitée par Lasilix®. Je vais décompresser enfin. J’espère en obtenir une petite rémission, une ‘’suspension’’ de peine de cette satanée Delta…
Par contre, ma vie est en rémission totale sous interféron, je ne sors plus, je ne vais plus aux réunions de mon association (ACT-UP), je suis détaché du sexe car je n’ai plus de libido, je m’isole, je deviens ‘’un croisé qui fait la guerre à la Delta’’ et je travaille.
D’après mes examens, j’ai une hypothyroïdie, la testostérone dans les chaussettes et on me surveille un petit nodule au foie par IRM et marqueurs biologiques.
Je suis sur une liste pour une transplantation depuis cinq ans, j’ai fait toute la batterie d’examens pour, mais je n’ai pas envie de la faire maintenant car elle me parait lourde et risquée. Je préfère attendre des nouvelles molécules et surtout, j’attends beaucoup des thérapies par cellules souches qui sont en développement aux Etats-Unis et en Corée. J’espère tenir jusqu’à leur arrivée, à coups de traitements et de ténacité.
Stéphane P
(1) CHV = Collectif interassociatif Hépatites Virales, groupant huit associations militantes (hépatites et Sida)
(2) 1ere conférence européenne de consensus de la co-infection (VIH-Hépatites), 1 et 2 mars 2005, Paris.
(3) Farci P, Roskams T et al. Long-term benefit of interferon alpha therapy of chronic HDV: Regression of advanced hepatic fibrosis. Gastroenterology 2004;126:1740-9.
(4) Castelnau C et al, abstract 1174. AASLD 2004 Et
Castelnau C et al. Efficacy of peginterferon alpha-2b in chronic hepatitis delta: Relevance of quantitative RT-PCR for follow-up. Hepatology 2006;44:728-35.
(5) Erhardt A, Gerlich W et al. Treatment of chronic hepatitis delta with pegylated interferon-alpha2b. Liver Int 2006;26:805-10.
(6) Niro GA, Ciancio A et al. Pegylated interferon alpha-2b as monotherapy or in combination with ribavirin in chronic hepatitis delta. Hepatology 2006; 44:713-20.
(7) Wedemeyer H, Yurdaydin et al. 72 week data of the HIDIT-1 trial : A randomised study comparing peginterferon alpha-2a plus adefovir vs. peginterferon alpha-2a plus placebo vs. adefovir in chronic delta hepatitis. J Hepatol 2007;46 (Suppl. 1):S4.
(8) Lamers M, Kirgiz O et al. Interferon-α for patients with chronic hepatitis delta: a systematic review of randomized clinical trials. Antivir Ther. 2012 Aug 15; 22892440